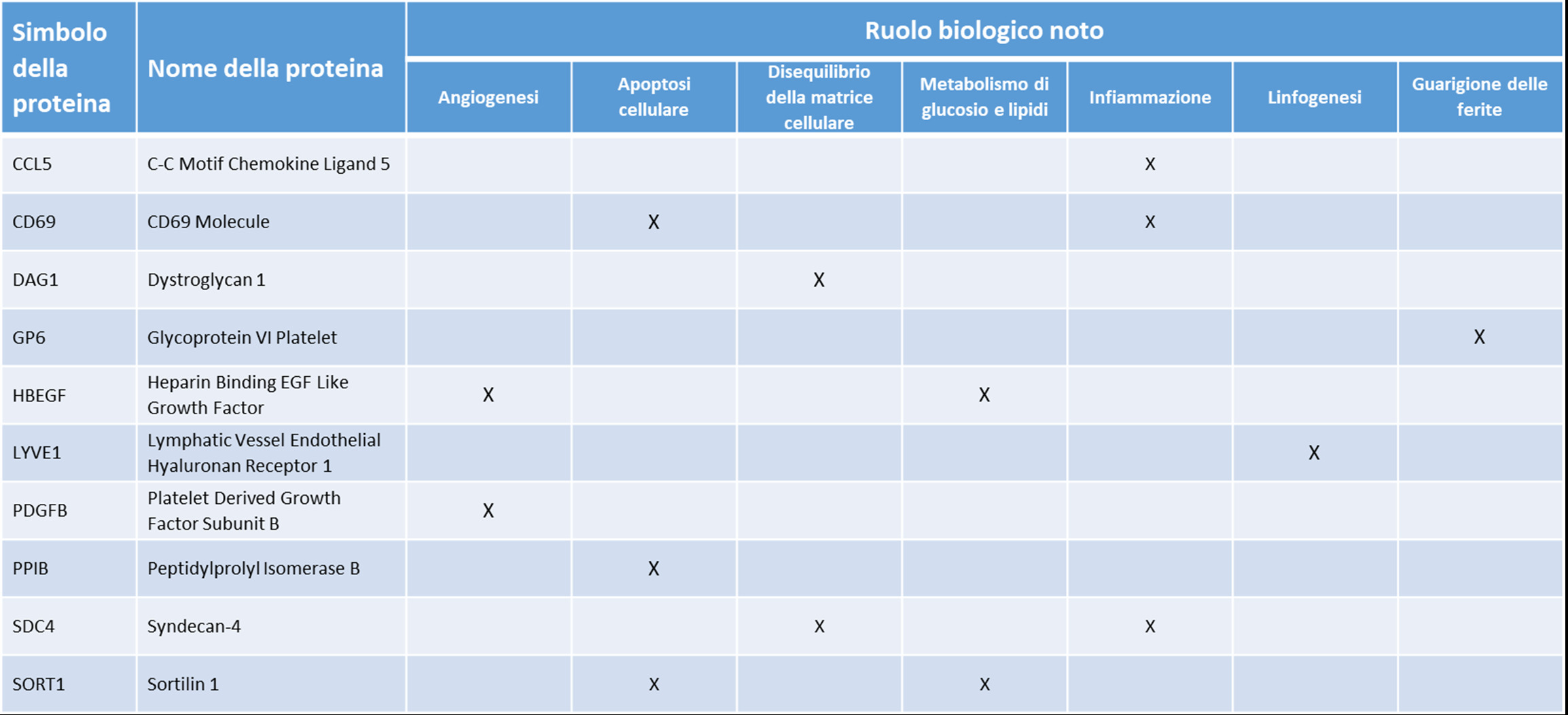
La disfunzione β-cellulare è un aspetto cruciale del deterioramento glicemico nel diabete tipo 2 (DM2). Non è noto se ci siano proteine circolanti in grado di spiegare l’aggravarsi nel tempo di tale disfunzione. A questo scopo, abbiamo studiato 639 pazienti DM2 di diagnosi recente, bianchi nord-europei, seguiti con lo studio prospettico e multicentrico IMI DIRECT. Abbiamo stimato la sensibilità al glucosio della β-cellula (GS) da test di pasto misto ai mesi 0, 9, 18, e 36, ed abbiamo modellato tali dati con una funzione lineare del tempo, la cui pendenza indica la progressione di GS (GSp). Al mese 0, abbiamo misurato 459 proteine in plasma EDTA a digiuno, usando pannelli Olink (Metabolic, Cardiometabolic, Cardiovascular II e III, e Development). Le proteine sono state aggiustate per centro, stagionalità, piastra, ora del giorno, ed età del campione. Abbiamo studiato le associazioni tra GSp e proteine con modelli di regressione lineare di GSp aggiustati per la prima componente principale dei dati proteomici, l’assunzione di farmaci con riportati effetti sulla glicemia, ed alcuni tratti clinici basali (sesso, età, BMI, GS, attività fisica, e HbA1c). Dieci associazioni sono risultate statisticamente significative (FDR<0.1), con R2 parziale tra 0.016 e 0.022, e sono mostrate in tabella. Il modello di regressione lineare aggiustato che include tutte le 10 proteine ha R2 aggiustato 0.159 (0.134 senza proteine). I principali processi biologici in cui le proteine selezionate sono coinvolte riguardano potenzialmente la secrezione di insulina (tabella). La nostra analisi 1) suggerisce un potenziale ruolo di proteine specifiche nella progressione della disfunzione β-cellulare, seppur modesto; 2) incoraggia l’analisi dei dati a disposizione, insieme ai dati proteomici longitudinali dello studio IMI DIRECT, con ulteriori metodi di analisi, come l’analisi funzionale, al fine di esplorare i meccanismi della disfunzione β-cellulare nel DM2.